时间:2020-07-27 09:04 │ 来源:医药云端工作室 │ 阅读:2244
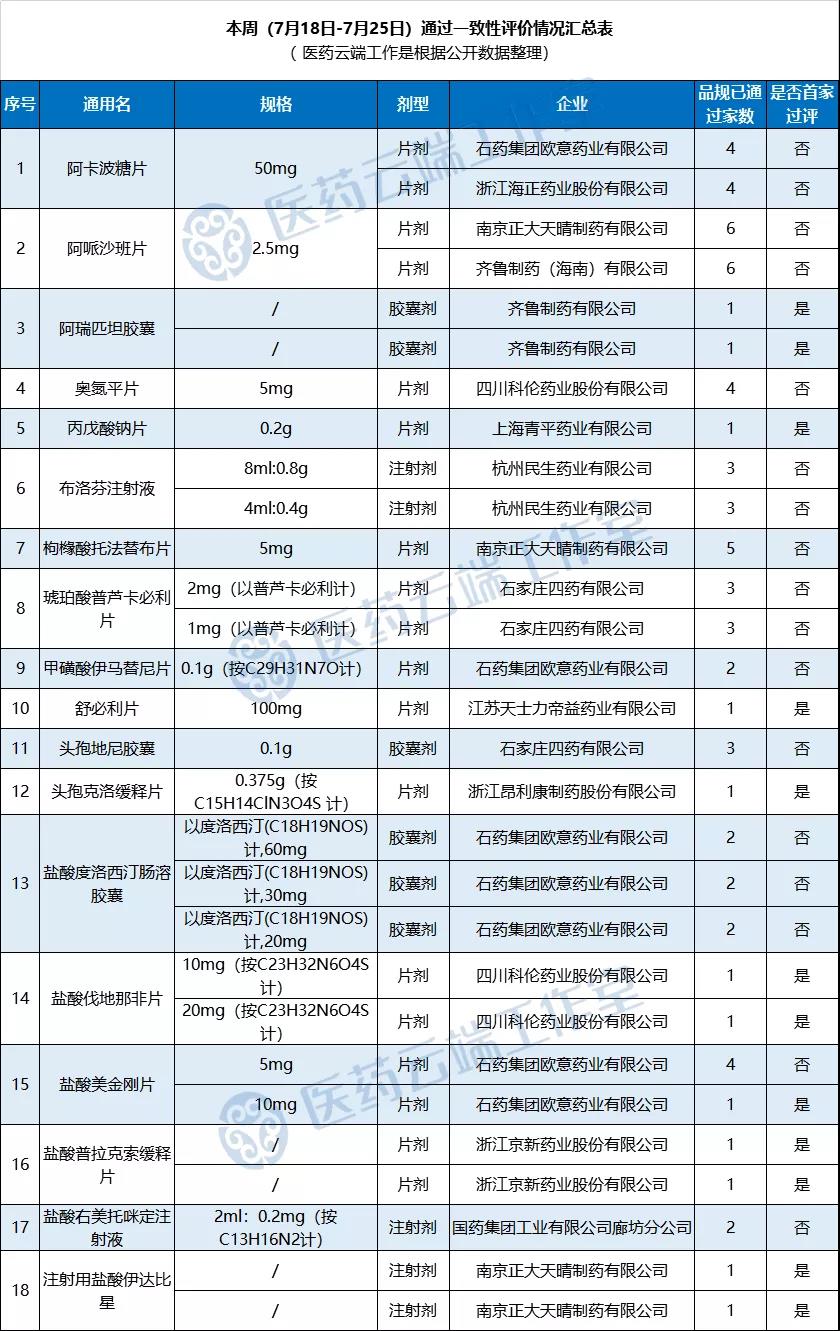
根据医药云端工作室统计,2020年7月20日-2020年7月26日,新增18个品种通过一致性评价,具体如下表:
南京正大天晴:阿哌沙班片、枸橼酸托法替布片、注射用盐酸伊达比星获批,视同过评
枸橼酸托法替布(枸橼酸托西替尼)是辉瑞研发的一种JAK抑制剂,可有效抑制JAK1和JAK3的活性,阻断多种炎性细胞因子的信号转导,对类风湿关节炎、溃疡性结肠炎、银屑病等多种炎症相关疾病有良好的治疗效应。
值得注意的是,在 2018 年 8 月 13 日,正大天晴专利挑战成功,辉瑞 JAK 抑制剂托法替布核心专利-化合物专利被宣告全部无效;其晶型专利(公开号:CN1596257A)于 2022 年到期。
国工有限:盐酸右美托咪定注射液(2ml:0.2mg(按C13H16N2计))获批,视同过评
7月24日,现代制药发布公告其全资子公司国药集团工业有限公司盐酸右美托咪定注射液获批,且视同过评。
盐酸右美托咪定注射液主要用于行全身麻醉的手术患者气管插管和机械通气时 的镇静。
该药品由 Abbott Laboratories(美国)和Orion Pharm(芬兰)共同开发研 制,于1999年12月首次获得美国FDA批准上市。
CDE网站显示,盐酸右美托咪定注 射液国内已有江苏恒瑞医药股份有限公司、辰欣药业股份有限公司、江苏恩华药业 股份有限公司等10家企业获批上市;目前该药品视同通过一致性评价的公司为国工有限及扬子江药业集团有限公司。
根据米内网数据库显示,盐酸右美托咪定注射液 2019年在全国城市样本公立医院的销售额为人民币28.72亿元。
公告显示,截至目前国工有限在该项目中累计投入研发费用约人民币641.36万元(未经审计)。
昂利康:头孢克洛缓释片( 0.375g)通过一致性评价
近日,浙江昂利康制药股份有限公司的头孢克洛缓释片(规格 0.375g)已通过一致性评价,且为全国首家过评。
头孢克洛缓释片是第二代头孢菌素类药物,原研厂商为美国礼来公司。该药品临床适用于敏感病原菌所致的下列感染:急性支气管炎和慢性支气管炎急性发 作、咽炎、扁桃体炎、肺炎、鼻窦炎、单纯性下尿路感染、皮肤软组织感染。
头孢克洛缓释片已被列入《国家医保目录(2019 年版)》,类别为乙类药品。
据公告显示,昂利康就该药品于 2019 年 04 月 22 日向国家药监局药品审评中心递交补充申请,于 2019 年 05 月 21 日获得受理。截至本公告披露日,公司对该药品一致性评价累计研发投入金额约为人民币 1,731.61 万元(未经审计)。
石药集团:甲磺酸伊马替尼片通过一致性评价,阿卡波糖片、盐酸美金刚片、
盐酸美金刚片
盐酸美金刚片是一种中重度阿尔茨海默症治疗药物。这是一款N-甲酰天冬氨酸受体拮抗剂,可以阻断神经功能异常导致的谷氨酸水平病理性升高,有效调控兴奋性递质,减缓神经退化过程,从而改善认知功能。该药品已被纳入2019年版国家医保乙类目录,限明确诊断的中重度至重度阿尔茨海默型痴呆。
目前盐酸美金刚片国内上市厂家主要为丹麦灵北制药和联邦制药,中标价中值分别为13.54和11.63元。2018年,联邦制药盐酸美金刚片销售额为4400万元。另外,联邦制药也在申请该药品的一致性评价。
除石药欧意外,目前还有广州白云山医药集团股份有限公司白云山制药总厂、湖南洞庭药业、安徽华辰制药三家企业的盐酸美金刚片已过评。
据医药魔方数据库显示,目前扬子江和长春海悦等在内的多家企业也在申报该品种一致性评价。石药欧意申报的盐酸美金刚片一致性评价因“海内外共线品种”于2019年2月被纳入优先审评程序。
甲磺酸伊马替尼片
伊马替尼已被纳入国家医保乙类目录,国内生产厂家除原研诺华外,还有豪森、正大天晴和石药集团。其中,豪森和正大天晴已率先通过一致性评价,并且在联盟地区带量采购中以10.38元/片和9.77元/颗的价格中标。
度洛西汀是礼来开发的一种选择性5-羟色胺(5-HT)和去甲肾上腺素(NE)再摄取抑制药。临床上主要用于治疗抑郁症。该药于2004年8月获得FDA批准,2006年8月在中国获批,商品名为欣百达。欣百达峰值销售额曾达到50.84亿美元,2019年,欣百达销售额为7.25亿美元。
石药集团的该药品按新4类提交获批后视同通过一致性评价。这是继倍特药业之后国内第2家该药品通过一致性评价的厂家。据医药魔方数据显示,按新4类提交度洛西汀肠溶胶囊的厂家还有重庆药友、齐鲁制药和东阳光等。
天士力:全资子公司药品舒必利片(100mg)通过一致性评价
近日,天士力之全资子公司江苏天士力帝益药业有限公司收到国家药监局颁发的关于舒必利片100mg 规格的《药品补充申请批准通知书》(通知书编号:2020B04047),该药品通过仿制药一致性评价,且为全国首家过评。
舒必利片用于精神分裂症,对抑郁症状有一定疗效,其他用途有止呕,为国家基本药物,并进入国家医保目录(甲类)。
截至本公告日,在中国境内有近百家企业获得舒必利片的批准文号,主要生产企业除江苏帝益外,还有恩华药业、广东彼迪药业和上海上药信谊药厂。
根据米内数据库,舒必利片 2019 年的城市公立医院年度销售为 4168 万元(城市公立 医院年度销售占比为 61.27%),2019 年年度增长率为 24.77%。
江苏帝益的该药品于 2019 年 8 月 12 日向国家药监局递交一致性评价申请,于 2019 年 8 月 19 日获得受理。截至公告日,江苏帝益针对该药品一致性评价已投入研发费用约为 556 万元人民币。
近日,齐鲁制药4类仿制药阿瑞匹坦胶囊和阿哌沙班片获得国家药监局批准上市,视同通过一致性评价,其中阿瑞匹坦胶囊为国内首仿。
阿瑞匹坦是一种高选择性P物质神经激肽1(NK1)受体拮抗剂,临床上适用于预防高度致吐性抗肿瘤化疗的初次和重复治疗过程中出现的急性和迟发性恶心和呕吐。
7月20日,杭州民生药业申报的3类仿制药布洛芬注射液获得国家药监局批准上市,同时视同通过一致性评价。此前已有成都苑东和吉林四环获批并视同过评,
为国内第3家该药品视同过评的企业。
据了解,布洛芬注射液是FDA唯一批准用于儿科解热、镇痛双适应症的非甾体注射剂。苑东生物的布洛芬注射液于2018年7月获批成人退热和镇痛。2019年7月,该药适应人群从成人扩展至6个月以上儿科患者。据苑东生物招股书显示,其布洛芬注射液2019年销售额为4979万元。
一直以来,围绕布洛芬注射液的布局显得竞争激烈。2014年度药品评审报告显示,待审评的品种中,布洛芬(注射剂)抢仿药扎堆申报严重,申报数量超过50件。这一结果也令业界感到意外,毕竟非甾体抗炎药的特点决定其更多适合用于口服和局部外用,布洛芬注射液的市场表现也有待观察。
布洛芬目前已获批上市的剂型有不下 20 种,Insight 数据库显示,其中文号在使用的有 549 个,涉及 372 家企业。
国内目前已有10余家企业通过布洛芬一致性评价。,其中胶囊剂、颗粒、片剂过评均已达到 3 家,且布洛芬缓控释剂、颗粒剂出现在此前业内流传出来的国家第三批集采报量名单中。
石四药:琥珀酸普芦卡必利片、孢地尼胶囊获批,视同过评
近日,石四药集团公告称其国内全资附属公司石家庄四药有限公司(石家庄四药)已取得国家药监局有关琥珀酸普芦卡必利片(1mg 及2mg)和头孢地尼胶囊(0.1g)的药品生产注册批件,两款药品均按新分类化学药品4类申请,获批后视同过评。
琥珀酸普芦卡必利片
琥珀酸普芦卡必利片主要用于治疗慢性便秘症状。琥珀酸普芦卡必利原研公司为美国强生,中国市场销售为强生在中国的子公司--西安杨森。
该药品是唯一被FDA批准治疗慢性便秘的新型促动力药,被众多指南和共识推荐为Ⅰ级循证医学证据和A级推荐,且被列入国家医保目录。
2018年11月17日,豪森申报的琥珀酸普芦卡必利片获批。豪森成为国内首家获批生产此药的公司。
2020年2月5日,河北仁合益康药业的静普欣®—琥珀酸普芦卡必利片获批,该产品用于治疗成年女性患者中通过轻泻剂难以充分缓解的慢性便秘症状。
石家庄四药是国内首三家已通过一致性评价的企业之一。
据悉,康美药业、济川药业等国内知名药企也分别在2018年10月、12月提交了琥珀酸普芦卡必利片的4类ANDA(仿制药上市)申请。
头孢地尼胶囊
头孢地尼是一种头孢类抗生素,主要用于治疗对头孢地尼敏感的葡萄球菌属、链球菌属、肺炎球菌、消化链球菌、丙酸杆菌、淋病奈瑟氏菌、卡他莫拉菌、大肠埃希菌、克雷伯菌属、奇异变形杆菌、普鲁威登斯菌属、流感嗜血杆菌等菌株所引起的各种感染,例如咽喉炎、扁桃体炎、急性支气管炎、肺炎等。
石家庄四药是国内仅有的三家已通过一致性评价的企业之一,按照新分类化学药品4类取得生产批件。除石家庄四药外,此前江苏豪森全国首家过评,而成都倍特药业的该品种以仿制药4四类申报,获批后视同过评。
据米内网数据显示,2019年中国公立医疗机构终端,头孢地尼是超30亿的重磅品种,在内服全身用抗细菌药通用名TOP20中排名第二。