2020年,中国首款贝伐珠单抗生物类似药上市第1年大卖18亿元,传统老牌药企齐鲁制药销售实力展露无遗。
有数据统计,2020年1~7月安维汀(贝伐珠单抗的原研药商品名)在全国样本医院销售额为13.75亿元,较上年同期下降9.9%,以此增速递推至全年约为26亿元。在贝伐珠单抗的战场中,国产生物类似药似乎已经赢了开端。据悉,罗氏的贝伐珠单抗于2004年首获FDA批准,2010年在中国上市用于治疗转移性结直肠癌,2015年被NMPA批准用于治疗非小细胞肺癌。如今,这两个适应证均已纳入2019年医保目录乙类报销范围。此外,该药还在中国获批了复发性胶质母细胞瘤、联合阿替利珠治疗既往未接受过系统治疗的不可切除肝细胞癌、以及HER2阴性转移性乳腺癌。相较之下,齐鲁的贝伐珠单抗(商品名:安可达)显得很年轻。2019年12月6日,该药获NMPA批准用于晚期、转移性或复发性非小细胞肺癌、转移性结直肠癌患者的治疗。适应证、经验均不敌原研的齐鲁如何“赢”在起跑线上?一个很重要的原因是进院能力。一方面,梳理原研药在医保目录中的历程可以看到企业“积极式的妥协”,给国产药增加难度;另一方面,在进入医保的前提下,传统药企如何结合自身优势利用现有条件将自己的药品快速入院,这是齐鲁做首仿药多年攒来的经验。仔细回顾,2017年7月,罗氏安维汀在江西的挂网价格为5223元/瓶,经过2017年医保谈判安维汀以60%的降幅进入,谈判价格为1998元/瓶。后续罗氏再次续约将价格稳在1934元/瓶。直至齐鲁制药安可达上市,2019年12月初挂网价格为1266元/瓶,后续降价至1198元/瓶。面临已上市的安可达和诸多排队上市的竞品,同年12月26日罗氏再次降价约22%,以1500元/瓶价格续约医保。医保局2019年65号文件规定,“在医保协议有效期内,如有同通用名药物(仿制药)上市,医保部门将根据仿制药价格水平调整该药品的支付标准,也可以将该通用名纳入集中采购范围”。凭借此政策,安可达以不到原研80%的价格快速入院,实现放量增长。据齐鲁知情人士透露,在安可达获批之前的一两年齐鲁制药便开始为该药招募团队。“进入医保,不一定意味着进入医院”,多位创新药药企代表曾反映医保落地最后一公里之难。对于生物类似药来说,如何在借力原研药铺垫的基础,譬如医生对药品的认知、进入医保等,实现自己的“野蛮”增长,这可能是传统药企已经积淀了多年的能力。再反观国内首个获批的生物类似药——利妥昔单抗(商品名:汉利康),优势似乎就没有那么明显。据财报数据,自2019年5月开出首张处方,汉利康7个月的总销售额约人民币1.9亿元,而罗氏原研药美罗华2019年样本医院销售额为24.54亿元。生物类似药究竟能否打败原研药实现快速替代?答案应该是肯定的,但需要的时间却由这些国产玩家来决定。目前参与生物类似药的主要有两类,一类是向创新转型的Bigpharma,一类是兼做生物类似药和创新药Biotech,他们之间的竞争则更为激烈。01 转型的Bigpharma VS 初生的Biotech从安可达18亿销售的“一斑”,足以窥生物类似药市场这一“全豹”。全球生物类似药市场规模正处于快速增长阶段,根据弗若斯特沙利文咨询公司发布的《中国生物类似药市场研究报告》数据显示,2018年全球生物类似药市场规模达72 亿美元,预计将于2030年达到1644亿美元。而中国的生物类似药市场也将于未来几年呈现爆发式增长,预计2030年可达到589亿元。对比化学仿制药,生物药研发和生产壁垒较高,我国在生物类似药方面的起步也较晚,在2019年之前中国尚未有国产生物类药获批上市。一面是广阔的未被满足的市场,一面是“同一起跑线”,向创新转型的Bigpharma与“初生牛犊”Biotech在此交锋。从2019年2月,NMPA批准了复宏汉霖的利妥昔单抗注射液开始,截止2021年2月23日,国内生物类似药共有5家企业的9款产品获批上市。
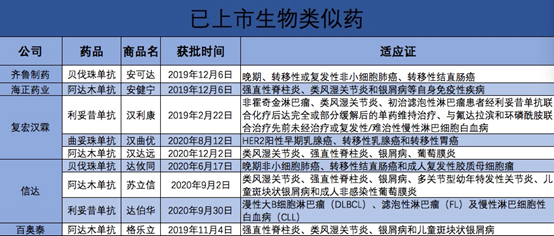
图片来源:根据CDE官网整理
从销售额来看,齐鲁制药的安可达一骑绝尘,取得了年销售额18亿的好成绩。根据PDB药物综合数据库统计,2020年Q1-Q3,百奥泰的阿达木单抗(商品名:格乐立)销售额为700万元,海正生物的阿达木单抗(商品名:安健宁)销售额为500万元。信达生物和复宏汉霖的生物类似药上市不久,也正在销售中。 从获批的产品数量来看,信达生物和复宏汉霖分别各以3款产品占据极大优势。而齐鲁制药和海正药业虽然在数量上不占优势,但在获批时间上却占据有利位置。前文我们也提到,复宏汉霖的利妥昔单抗(商品名:汉利康)虽是国内首个获批的生物类似药,占据了先发优势,但这并没有展现在销售额上。而齐鲁制药凭借其沉淀多年的渠道及销售经验,仅靠一款产品依旧可以大卖。从适应证数量来看,信达生物的贝伐珠单抗(商品名:达攸同)、阿达木单抗(商品名:苏立信)和利妥昔单抗(商品名:达伯华)分别已获批3个、6个、3个适应证。复宏汉霖的利妥昔单抗(商品名:汉利康)、曲妥珠单抗(商品名:汉曲优)、阿达木单抗(商品名:汉达远)分别已获批4个、3个、4个适应证。百奥泰的阿达木单抗(商品名:格乐立)已获批4个适应证。而齐鲁制药的贝伐珠单抗(商品名:安可达)获批2个适应证,海正药业的阿达木单抗(商品名:安健宁)获批3个适应证。从数量来看,以信达生物、复宏汉霖和百奥泰为代表的Biotech公司更具优势。而从适应证范围来看,各家公司均集中于肿瘤或自身免疫疾病上。生物类似药的竞争除了在抢占进入市场的时机上,还在服务市场的“后劲”——产能上。齐鲁制药和海正药业凭借在原料药和制剂方面多年的积累,在产能上略胜一筹。而信达生物、复宏汉霖和百奥泰则更为灵活。2020年11月,齐鲁制药再次与生物制药生产整体解决方案和服务供应商ABEC合作,以迅速扩大其cGMP生产工厂的产能。ABEC将交付数套大规模不锈钢细胞培养生物反应器。据悉,齐鲁先前安装的ABEC大规模生物反应器是目前中国运营中的最大的生物反应器。目前具体产能齐鲁制药未透露。 根据公司官网显示,信达生物目前已建成3条1000升产能的生产线和6条3000升产能的生产线,一共有2.1万升的产能。同时还有12条3000升的不锈钢生物反应罐正在建设中,总计共有20万升产能在建设规划中。复宏汉霖徐汇基地的商业化总产能为2万升,此外复宏汉霖正同步扩大松江基地(一)的产能建设,规划建设产能达2.4万升。百奥泰目前已完成建设并投入使用的有2套3500L不锈钢生物反应器及其配套的下游纯化生产线,3套500L一次性反应器及其配套的下游纯化生产线,1套200L抗体药物偶联体反应釜及其配套的隔离器系统及纯化生产线,1条西林瓶无菌注射液洗烘灌封联动生产线,1条预灌封注射器灌装生产线和1条冻干生产线。随着越来越多的企业参与到生物类似药的开发中,竞争激烈的同时,生物类似药的集采似乎箭在弦上。2月18日,年后第一个工作日,CDE官网发布《生物类似药相似性评价和适应证外推技术指导原则》,为生物类似药细分领域的产品研发和适应证外推使用正式提出明确的监管要求。政策到来得有点急促。业内分析认为,该政策的落地在为生物类似药集采铺平道路。实际上,更早之前政策频频释放了相关的信号。去年7月,国家医保局发布消息称,有关司室已就生物制品(含胰岛素)和中成药集中采购工作召开座谈会,研究完善相关领域采购政策,推进采购方式改革。接着10月,医保局对“十三届全国人大三次会议第6450号建议的答复”中明确,在考虑生物类似药的相似性、企业产能和供应链的稳定性、具体产品的临床可替代性等因素的基础上,适时开展集中带量采购。春节前,国家医疗保障局副局长陈金甫在国务院政策例行吹风会上也明确表示,生物类似药跟化药的仿制药质量评价方式上有差别,但是它有严格的质量标准,下一步纳入集采是毫无疑义的。而根据集采规则,只要满足同一通用名下原研药和仿制药数量大于等于3个,就可以展开集采。目前贝伐珠单抗和阿达木单抗均满足这一条件。另一方面,医药企业家们关于生物类似药集采的建议也侧面反映了事情的急迫性。多家企业代表普遍认为,目前我国生物制剂/生物类似药在相似性、产能和供应稳定性、替代性方面还需积累更多的经验,不完全满足纳入国家带量采购的前提条件。针对生物制品的采购政策希望能够统筹考虑,充分考虑生物制剂产品特点、产业发展阶段、临床需求和患者安全,降低大规模替换带来的潜在用药安全风险,探索适合生物制品的创新采购政策,实现患者用药安全、医保控费和产业发展的三赢局面。


