免疫代谢(immunometabolism)涉及糖酵解、三羧酸循环、磷酸戊糖途径和氨基酸代谢等细胞内代谢通路网络,在调节免疫细胞反应中起着至关重要的作用。特别是,氨基酸,如色氨酸(Trp)、精氨酸、谷氨酰胺和亮氨酸的代谢可以影响肿瘤的进展和免疫细胞的增殖和分化。因此,通过调控与这些氨基酸代谢相关的酶,科学家们一直在尝试开发免疫代谢癌症疗法。不过,靶向这类酶的传统小分子抑制剂因为耐药性的存在,通常无法产生持久的响应,此外,一些不可成药的酶无法被传统的小分子抑制剂靶向,因此,急切需要探索干预氨基酸代谢的替代方法。
PROTAC全称为Proteolysis-Targeting Chimeras,即蛋白水解靶向嵌合体,是一种不同传统小分子抑制剂的新药物类型,由3部分组成:靶蛋白binder、linker以及E3泛素连接酶binder,通过泛素-蛋白酶体系统介导靶蛋白的降解,提供了另一种调节蛋白稳态的方法。具体来说,PROTAC分子的一端与靶蛋白结合,另一端与E3泛素连接酶结合。而E3泛素连接酶可通过将一种叫做泛素的小蛋白贴在靶蛋白上将其标记为缺陷或受损蛋白。之后,细胞的蛋白粉碎机(即,蛋白酶体)会识别和降解被标记的靶蛋白。基于这种作用机制,基于PROTAC技术研发的药物也被称为蛋白降解剂。
PROTAC技术最大的优势之一是能够使靶点从“无成药性”变成“有成药性”。传统的小分子抑制剂需要与目标蛋白有很强的结合,通常是与活性位点结合,然而,据估计,人类细胞中80%的蛋白缺乏这样的位点。由于PROTAC只需要与目标蛋白弱结合就可以特异性地“标记”它,因此,目前蛋白质组中~80%不可成药的蛋白可能都能够用PROTAC技术来解决。
克服传统小分子抑制剂的耐药性是PROTAC技术的另一潜在优势。以AR靶点为例,大多数接受AR抑制剂恩扎卢胺治疗的患者会因为癌细胞产生AR突变等情况产生耐药性。而靶向AR的PROTAC可能能够催化多种突变蛋白的降解,从而在一定程度上克服或减少耐药性的产生。
到目前为止,PROTAC已被用于靶向多种蛋白,被研究较多的靶点包括AR、BTK、BRD2-4、CDK4/6等。然而,用PROTAC来靶向免疫代谢相关蛋白的研究并不多。

5月18日,最新发表在Nature Communications杂志上的一项研究中,来自新加坡南洋理工大学的一个科学家团队开发了一款可智能激活的靶向吲哚胺2,3-双加氧酶(Indoleamine 2,3-dioxygenase, IDO)的新型PROTAC——半导体聚合物纳米PROTAC(semiconducting polymer nano-PROTAC, SPNpro)。研究证实,SPNpro巧妙结合了光学疗法抗癌和蛋白降解抗癌两重力量, 高效抑制了小鼠肿瘤生长和转移。同时,该研究通过在肿瘤中特异性激活PROTAC克服了当前PROTAC分子潜在的脱靶副作用。
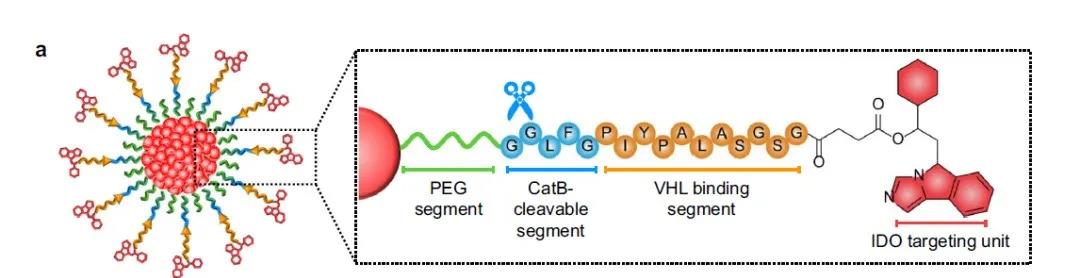
SPNpro的结构(来源:Nature Communications)
SPNpro由一个半导体聚合物核(semiconducting polymer core)通过一个癌症生物标志物可切割肽(cancer-biomarker-cleavable peptide)偶联PROTAC片段组成。半导体聚合物纳米颗粒(Semiconducting polymer nanoparticles, SPNs)具有良好的生物相容性和可调的光学特性,因此被科学家们用于光学疗法的开发。吲哚胺2,3-双加氧酶(IDO)被选作PROTAC的靶蛋白是因为,该酶是一种在肿瘤组织中过表达的色氨酸分解酶,可将色氨酸转化为犬尿氨酸(Kyn),导致树突状细胞(DC)功能障碍和效应T细胞的功能抑制。靶向IDO的PROTAC肽(IDO-targeting PROTAC peptide, IPP)由被广泛使用的IDO抑制剂NLG919与E3泛素连接酶VHL 结合肽连接而成。组织蛋白酶B (Cathepsin B, CatB)被选为癌症生物标志物,它通常在多种癌症细胞中过表达,如乳腺癌、结直肠癌、黑色素瘤和前列腺癌。
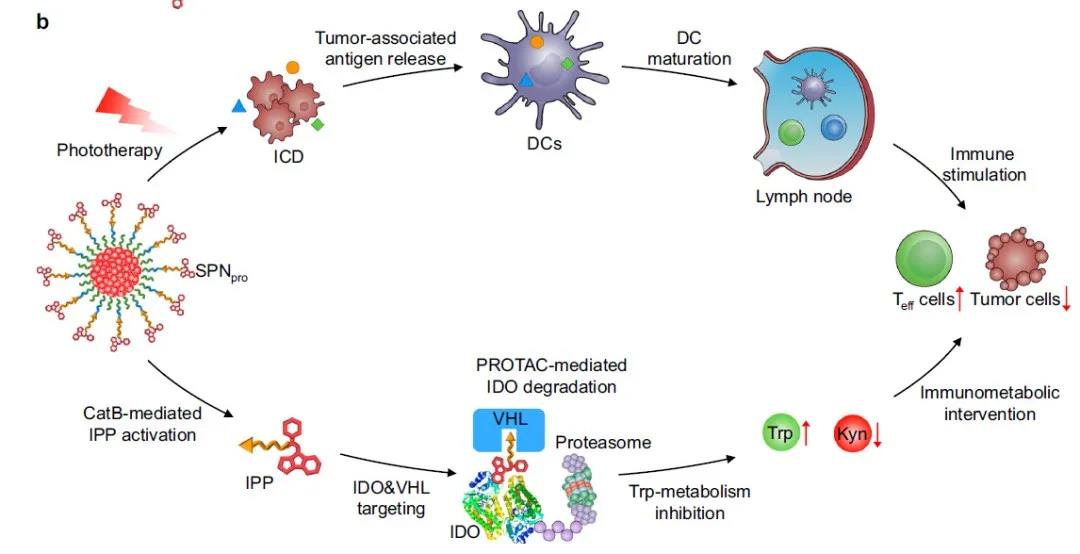
SPNpro介导IDO降解的示意图 | SPNpro通过两个过程介导激活的光免疫代谢疗法(activatable photo-immunometabolic therapy):(i)通过近红外光照射,产生一系列癌症免疫反应,如免疫原性细胞死亡(ICD)、肿瘤相关抗原释放、DC成熟和效应T (Teff)细胞激活;(ii)SPNpro介导了免疫代谢干预过程,包括CatB特异性激活IPP、IDO和VHL靶向、蛋白酶体募集、IDO降解、色氨酸上调和Kyn消耗以及Teff细胞激活。(来源:Nature Communications)
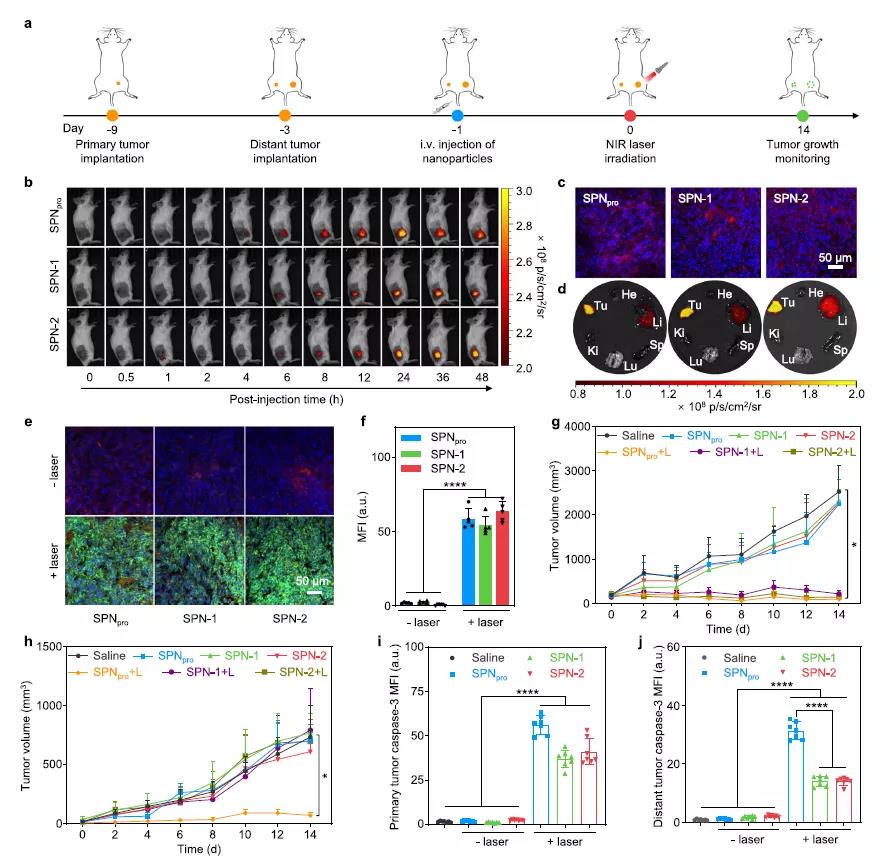
SPNpro发挥作用的具体机制如下:一方面,系统性给药后,SPNpro可在被动地在活鼠肿瘤中积累,在近红外光照射下产生单线态氧,以消除肿瘤细胞,诱导肿瘤相关抗原的释放和免疫原性细胞死亡(immunogenic cell death, ICD)。这些释放的肿瘤相关抗原进一步诱导DC成熟,促进T细胞活化,进而增强抗肿瘤T细胞免疫应答。
在体内,SPNpro介导了可激活的光免疫代谢疗法(activatable photo-immunometabolic therap)(来源:Nature Communications)
同时,SPNpro的PROTAC功能可被癌症生物标志物CatB特异性激活。在活鼠中,肿瘤表达的CatB可原位裂解SPNpro并释放靶向IDO的PROTAC肽(IPP)。激活的IPP与免疫抑制性IDO结合,进而诱导其降解。IDO降解可缓解色氨酸过度消耗和犬尿氨酸(Kyn)积累,从而逆转免疫抑制,促进效应T细胞的激活。最终,SPNpro介导的原位免疫代谢干预协同免疫原性光学疗法有效增强了抗肿瘤T细胞免疫反应,抑制了肿瘤生长和转移。总结来说,该研究为对抗癌症提供了一种新的联合治疗模式。同时,通过SPNpro这种设计,科学家们在解决传统PROTAC持续起作用(always-on bioactivity)和脱靶副作用方面取得了新的进展。此外,这类PROTAC设计也可以用于其它免疫代谢相关的靶蛋白,如谷氨酰胺酶、精氨酸酶、脂肪酸合成酶、乳酸脱氢酶和乙酰辅酶A乙酰转移酶,为PROTAC在癌症治疗方面的发展提供了新的机遇。