近日,工信部发布了《四部门关于加强短缺药品和国家组织药品集中采购中选药品生产储备监测工作的通知》,通知要求地方工业和信息化主管部门会同卫生健康、医疗保障、药品监管主管部门对1236家短缺药品生产企业和783家国家集采中选药品生产企业进行生产储备监测,监测企业目录实施动态调整。
值得注意的是,虽然目录中783家药品生产企业并非全部国采中选药品生产企业,但被监测的国家集采中选药品不仅涉及第一批到第五批集采药品,还涉及第六批胰岛素集采的药品。在企业规模方面,齐鲁、扬子江、科伦等本土大药企,GSK、诺和诺德、拜耳等跨国药企也赫然在列。这也是首次如此大规模的由工信部会同卫健委、医保局、药监局,四部门联合对国家集采药品生产企业进行药品生产储备监测工作。E药经理人从相关企业获悉,企业所填报的信息不仅包括药品信息、药品供应量信息、药品院内销量信息,还包括核心原辅料供应情况、核心原辅料价格情况,以及中选地区的回款率、回款金额等涉及到中选企业(药品生产企业)保障药品供应、稳定药品供应价格的相关信息。事实上,如果将此前第三批集采中增加的“违规名单”机制,以及第七批集采加入的“替补机制”视作保障国采药品供应的后置手段,那么本次要求783家国家集采药品生产企业每月10日前填报监测报表,则更像是将“风险规避”前置化,从企业回款、原辅料供应等情况来保障药品供应。
01 断供,经营之困
自2018年开展带量采购以来,国家或各地方集采中,中选产品断供、停产问题时有发生。华北制药、百奥药业、山德士等20余家企业,都曾出现过集采中选后断供的情况。
药企断供往往与产能或价格因素有关。普遍来看,药企断供的风险主要来自于原材料大幅上涨导致无法继续按照中选集采价格供货;或是生产线出了问题,工厂停产或减产无法供应。
中选后断供带来后果是严重的。去年9月,国家医保局发布价格招采信用评价“严重”和“特别严重”失信评定结果(第1期),其中第三批国家组织药品集中采购品种布洛芬缓释胶囊的中选企业华北制药在山东省未能按协议供应约定采购量,华北制药被列入“违规名单”,取消华北制药自2021年8月11日至2022年5月10日参与国家组织药品集中采购活动的申报资格。
同样因为断供被列入严重失信的还有百奥药业。2021年9月,河南省公共资源交易中心发布公告称,百奥药业的恩替卡韦片为国家组织药品集中采购试点扩围中选品种,在河南省多次出现配送率低等供应问题,2021年5月至6月更是出现停产、断供等问题,且均未提前告知集中采购机构及采购单位。依据相关文件规定,百奥药业在河南省医药价格和招采信用失信等级评定为“严重”。百奥药业表示,恩替卡韦断货的原因主要是疫情、原料药涨价、断货等原因导致产能不足。
即使断供导致的处罚十分严苛,但对药企而言,断供也是无奈之举。
在2020年11月开启的浙江省首批带量采购工作中,东瑞制药从18家企业中突围并独家中选“注射用头孢美唑钠”(粉针剂,规格1.0g),但到了2021年3月,东瑞制药拒绝履行中选义务,未完成签订购销协议和建立配送关系等工作,影响中选结果的正常执行。
突出重围的东瑞制药为何冒着失信的风险也拒绝履行中选义务?公开信息显示,由于原料短缺的原因,东瑞制药已停止供应注射用头孢美唑钠。“没有原料,注射用头孢美唑钠无法生产,也没有明确的恢复供应时间。”曾有东瑞制药销售负责人公开表示。
成本与集采价格的变动极有可能造成集采产品断供。悦康药业也曾因未按议定价格和规定供应鱼精蛋白而被辽宁省医保局公示,在解释断供原因时悦康表示,原料成本上涨导致之前的“谈判价格根本执行不了。”长期以来,原料短缺或价格上涨已经是企业生产中无法逾越的一座大山。一方面,集采已经很大程度挤压了药品的利润,另一方面,原料药涨价可能导致药企无法收回成本,最终加剧断供风险。“原料药厂和制剂企业都无法接受。”原料药价格上涨,药企若以高价采购原料药,再以集采中选时的价格卖出,或是原料药企以低价出售原料给药企,双方都面临着连成本都达不到的现实。自2020年以来,因原料药价格上涨导致的集采中选药品断供情况时有发生。在压缩的利润空间与上涨的原料价格中间,很多药企不得不选择停产或退出。除了原料上涨导致的风险因素外,医疗机构回款周期长、回款率低也是困扰集采中选企业经营的一大风险因素。国内某省医药采购平台统计数据显示,该省份绝大多数地区30天内回款的金额不足20%,并出现大量逾期未回款现象,逾期未回款金额占总集采金额的接近一半。曾有回款现状调研显示,公立医疗机构药品回款账期最长达960天,欠款金额最高达8600万元。无法定期拿到回款给企业带来巨大的经营压力,影响后续生产。对此,国家医疗保障局副局长陈金甫在今年2月国新办召开的政策例行吹风会上进一步明确了集采回款的重要性。他表示,医疗机构采购药品必须确保回款。为了解决医疗机构资金紧张问题,医保基金预付30%,同时国家医保局也在探索,招采平台上跟药品配送企业和药品供应企业直接结算,让平台服务于企业,减少运营成本。同时,国家医保局也允许一些地方进一步扩大医保垫付药款的份额,同时在竞价规则里面,越来越对医疗机构还款作出了严格要求,同时通过开发软件系统来监督药品回款的进程。这些问题,或许都将通过监测平台的大数据监测与分析得到缓解。根据通知,被纳入监测的集采中选药品生产企业,通过“短缺药品生产供应监测预警平台”,填报《国家集中采购药品生产供应监测报表》,据E药经理人从目录中企业获悉,《国家集中采购药品生产供应监测表》中,对中选企业相应产品的生产量、库存量、销售量均有明确的监测。针对集采中选企业库存的管理中,产品核心原、辅料供应与价格情况,生产线产能以及中选地区的销售回款情况一直是管理的重点。将这些数据纳入监测后,可以进一步实现从药品的生产阶段监测保供情况。业内认为,此次将集采中选药品生产企业纳入预警监控名单中,可以极大程度地实现风险前置。进一步防止因核心原料上涨、回款等问题导致的断供。有观点认为,被纳入监测对企业而言并非坏事。通知明确,地方工业和信息化主管部门将会同卫生健康、医疗保障、药品监管主管部门督促指导本区域内监测企业通过线上方式填报生产储备信息,协调组织生产供应。工业和信息化部将会同相关部门对生产储备信息进行分析、适时开展检查评估并公布相关情况,协调解决重大问题。换言之,当企业的核心原、辅料供应与价格情况,生产线产能以及中选地区的销售回款出现问题与波动,有可能会导致后续出现产能不足、断供的问题发生前,相关部门可以通过预警平台及时预判、干预、协调,甚至是启动储备机制,避免造成断供等严重后果。其实,针对国采产品的保供制度早在“4+7”试点时便已经展开了。中国药科大学国家药物政策与医药产业经济研究中心执行副主任、药品监管科学研究院执行院长邵蓉此前表示,针对企业中选后的生产、配送环节,通过建立企业库存和停产报告制度,要求企业核算产能并上报。早在“4+7”试点时,相关部门就已规定各中选企业应每季度向联采办报送中选药品的库存数量,后续的国采中,同样要求中选企业每月向联采办报送库存数量。国家药品集采执行情况监测工作也自2019年5月启动,由医保部门牵头,协调区域内药品采购平台等按月进行数据收集、审核、汇总、分析及报送工作,保障供应方面的监测指标主要包括生产环节的生产库存、停复产、核心原辅料供应及价格,以及流通环节的地区库存及回款等情况。第七批集采已经明确为应对中选药企无法供应、停产等违约失信问题,确保临床使用稳定,首次引入备供机制,每个省份将同时有一个主供企业和一个备供企业。有观点认为,此次针对集采中选品种及生产企业的监测,也是在一定程度上保障此前六批七轮集采品种的稳定供应。事实上,除了上述提到的“违规名单”机制、“替补机制”等“追责”手段,国家和省际联盟集采中已经落实过多种保障药品供应、稳定药品价格的前置化手段。例如在全国第六批集采(胰岛素专项集采)中所设置的获得调出量规则以及在长三角联盟续约集采这种的综合评价体系规则。
在2021年进行的全国第六批集采(胰岛素专项集采)规则中明确规定了“当中选产品对应的企业获得的基础量和分配量总和超过其承诺供应国内市场最大产能的50%时,医药机构不得继续将调出量分配给该企业。”国家医保局在胰岛素集采当天接受央视采访时表示,“生物药与化药相比,生产周期较长,产能爬坡提升较慢,为确保供应,此次中选规则中规定,协议采购量不能超过最大产能的50%,从而确保中选企业产能充足。”2022年上半年,由上海、浙江、安徽组成的长三角联盟进行了集采续约,在续约规则中引入了类似“双信封”的规则——综合评价体系。长三角联盟的综合评价体系中尤其强调“信用和履约评价”,例如在企业药品保障供应能力设置25分,考核企业的行业排名、品种连续销售年份等指标。而若企业综合得分相同,“2021年在联盟地区销售量大的企业优先,多个规格的品种,销售量合并计算(以各地报送数据为依据)”则是附加考核指标之一。”
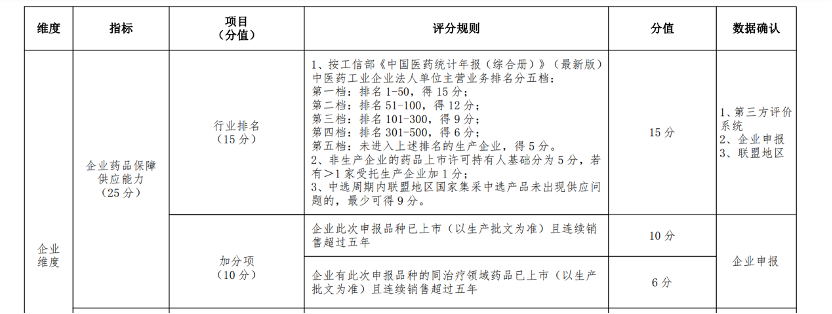
图表来源:《长三角(沪浙皖)联盟地区药品集中采购文件》
事实上,2021年11月国家医保局发布的《国家医疗保障局办公室关于做好国家组织药品集中带量采购协议期满后接续工作的通知》就明确了,稳定市场预期、稳定价格水平、稳定临床用药。分类开展接续。着眼于维护市场和临床用药稳定,综合考量企业和产品的多方面因素,通过询价、竞价、综合评价等方式确定中选企业和中选价格。业内人士认为,长三角联盟的综合评价体系对于集采续标的稳定性有重要的意义。
参考资料:中国医疗保险《带量集采:如何确保药品供应充足不断?》


